Découvrez la transcription de notre webinaire Post-ASH 23 avec le Dr. BLIN avec le Dr. BLIN, qui fournit une couverture complète de plusieurs études clés liées aux syndromes myélodysplasiques (SMD) à partir de la base de données de l'OMS sur les syndromes myélodysplasiques. Congrès ASH23. Le Dr BLIN se penche sur les spécificités de chaque étude, en discutant de leur conception, des caractéristiques des patients, des principaux résultats et des implications pour le traitement du SMD. Vous trouverez ci-dessous une transcription condensée de l'essentiel de chaque étude abordée dans la vidéo !
Syndromes myélodysplasiques
Le Dr BLIN aborde deux résumés essentiels du congrès ASH23 relatifs au traitement des syndromes myélodysplasiques (SMD), en se concentrant sur les avancées et les résultats des essais cliniques qui pourraient potentiellement changer le paysage thérapeutique pour les patients atteints de SMD.
COMMANDS : Analyse complète de l'essai de phase III comparant le Luspatercept à l'Epoetin alfa dans le traitement des SMD à faible risque, dépendants des transfusions et n'utilisant pas d'ASE.
- Conception de l'étude : L'étude COMMANDS est une étude de phase 3 comparant le luspatercept (LP) à l'époétine alpha (EPO) chez des patients atteints de SMD à faible risque, n'ayant jamais reçu d'agent stimulant l'érythropoïèse (ASE) et dépendant des transfusions.

- Population de patients : 360 patients ont été recrutés, présentant un SMD à risque très faible, faible ou intermédiaire selon l'IPSS révisé, en se concentrant sur ceux dont le taux d'érythropoïétine sérique endogène (EPO) était inférieur à 500 unités par litre.
Principaux résultats
- Efficacité : Le luspatercept est significativement plus efficace que l'époétine alpha pour ce qui est de l'indépendance vis-à-vis des transfusions de globules rouges (GR) pendant plus de 12 semaines, avec une augmentation moyenne simultanée de l'hémoglobine de plus de 1,5 g/dl à la semaine 24. Ce bénéfice a été observé chez différents groupes de patients, en particulier chez les patients présentant des sidéroblastes en anneau (RS), pour lesquels luspatercept a montré un avantage marqué.
- Critères d'évaluation secondaires : Les principaux critères d'évaluation secondaires, notamment l'amélioration hématologique et la réduction des besoins transfusionnels, ont favorisé le luspatercept par rapport à l'EPO à différentes échéances. La durée de l'indépendance transfusionnelle atteinte dans le groupe luspatercept était particulièrement impressionnante, suggérant des améliorations potentielles de la qualité de vie des patients.
Les résultats de l'étude COMMANDS soulignent l'efficacité du luspatercept dans la prise en charge des patients atteints de SMD à faible risque de dépendance transfusionnelle, en particulier ceux présentant des sidéroblastes en anneau. Sa supériorité dans l'obtention de périodes plus longues d'indépendance transfusionnelle et les améliorations potentielles de la qualité de vie font de luspatercept une avancée significative dans le traitement du SMD.
Analyse de sous-groupe de la phase III d'IMerge : Imetelstat pour l'atteinte de l'indépendance transfusionnelle chez les patients atteints d'un SMD à faible risque, admissibles ou non aux ASE.
L'essai de phase 3 d'Imerge est une étude importante axée sur l'efficacité de l'imetelstat, un inhibiteur de télomérase, dans le traitement des patients atteints de syndromes myélodysplasiques (SMD) qui sont soit réfractaires aux agents stimulant l'érythropoïèse (ASE), soit inéligibles à ces derniers en raison de taux sériques élevés d'érythropoïétine (>500 mU/mL).
Vue d'ensemble
- Conception de l'étude : Cet essai a recruté 178 patients dans le cadre d'une randomisation 2:1 pour comparer l'imetelstat au placebo. La stratification était basée sur la charge transfusionnelle et la catégorie IPSS-R. L'imételstat a été administré par voie intraveineuse toutes les quatre semaines, les patients recevant également des soins de soutien au besoin.
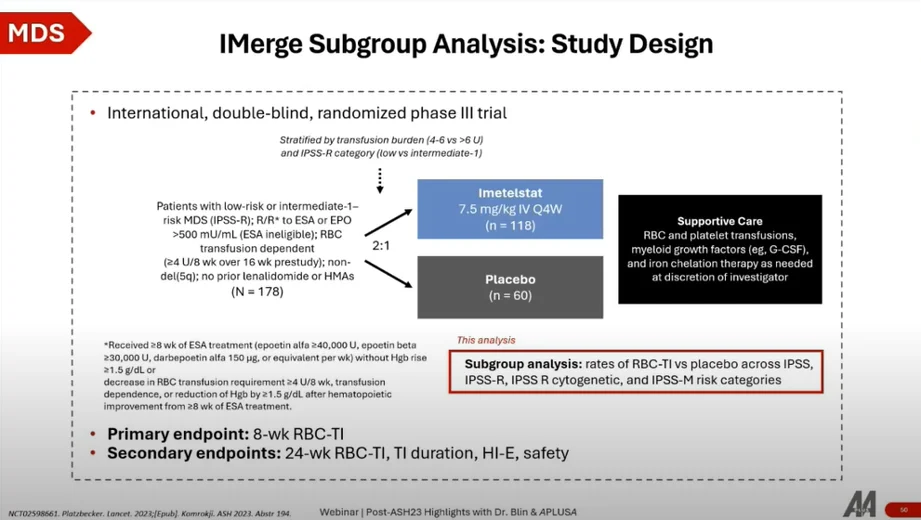
- Population de patients : Cible : patients atteints de SMD en deuxième intention ou plus tard, en particulier ceux qui ne répondent pas ou rechutent après un traitement par ASE, ou patients en première intention dont les taux sériques d'érythropoïétine indiquent qu'ils ne sont pas éligibles aux ASE.
Principaux résultats
- Efficacité : L'Imetelstat a démontré un net avantage dans l'obtention d'une indépendance transfusionnelle durable par rapport au placebo, à divers moments (semaines 8, 16 et 24), soulignant son potentiel en tant qu'option thérapeutique efficace.
- Catégories de risque IPSS-R : La réponse à l'imetelstat a été significativement meilleure dans les catégories de risque IPSS-R faibles à intermédiaires, sauf dans le groupe à faible risque, à des échéances plus longues, où la différence n'était pas statistiquement significative.
- Catégories de risque moléculaire : En utilisant l'IPSS-M de nouvelle génération, qui incorpore des mutations à haut risque comme TP53, l'imetelstat a montré une supériorité par rapport au placebo dans l'amélioration des résultats dans tous les sous-groupes de risque moléculaire, affirmant ainsi sa large applicabilité.
L'essai Imerge positionne l'imetelstat comme une nouvelle norme de soins potentielle pour les patients atteints de SMD à faible risque et dépendants des transfusions, qui ont des options limitées en raison de la réfractarité ou de l'inadmissibilité aux ASE. Les résultats indiquent que l'imetelstat pourrait offrir un avantage clinique significatif, soulignant la nécessité de poursuivre la recherche, éventuellement par des essais de phase 3, afin d'établir pleinement son rôle dans les paradigmes de traitement du SMD. Cet essai souligne l'évolution du traitement du SMD, axé sur des thérapies ciblées qui s'attaquent à des mécanismes spécifiques de la maladie.
Si vous avez manqué nos sessions précédentes sur le myélome multiple, le lymphome diffus à grandes cellules B et la leucémie myéloïde aiguë, vous pouvez maintenant lire nos articles de blog en cliquant sur les boutons ci-dessous :





